 14
14
各种空气洁净度级别洁净室的空气净化处理均应采用初效、中效、空气过滤器过滤。对于A/B/C级洁净室的末端过滤器效率应采用大于或等于99.95%(MPPS/H13)~大于或等于99.995%(MPPS/H14)。根据国际制药工程协会(ISPE)基准指南-无菌药品生产设施及国外相关文献的描述,单向流系统内的HEPA过滤器效率应为99.99%(IEST/H13/DOP或PAO),其完整性扫描检漏*必须在99.99%以上;对于B级区至少采用效率应为99.97%的HEPA过滤器,但其完整性扫描检漏*需在99.99%以上。
1.2.2 本条规定了净化空气调节系统中各级空气过滤器设置的几项原则。
1 中效空气过滤器宜集中设置在净化空气处理机组的正压段,因为考虑到负压段来自机组外空气的渗漏,会造成未经中效空气过滤器过滤的污染空气进入系统,增加了空气中的含尘浓度,加大下游空气过滤器的过滤负担,缩短其使用年限。
2 净化空气调节系统的HEPA过滤器安装位置通常布置在系统末端送风口处或集中设置于AHU末端。HEPA过滤器设置系统末端主要优点是可将送风受到再污染的危险降到,所以本条建议HEPA过滤器设置于净化空气调节系统末端。
服务于无菌药品的净化空气调节系统,根据国际制药工程协会(ISPE)基准指南-无菌药品生产设施的描述“所有无菌生产分级区A/B/C的送风均应经过滤器处理,由于系统中HEPA过滤器安装的关键在于避免空气再次受到污染,因此对于B级及以上的净化级别,送风末端必须设置HEPA过滤器”,末端HEPA过滤器装置对于保证无菌区域整体性来说是非常重要的。
3 在回风、排风系统中,由于空气中往往带有粉尘等有害物质,为防止未经过滤处理的空气泄漏,污染周围环境,因此应将过滤器设置在回风、排风机的负压吸入端,既起到保护环境的作用,又起到保护风机的作用。
4 空气过滤器的额定风量是在一定滤速下的风量,设计中为了降低净化空气调节系统的系统总阻力,在选择空气过滤器送风口时,一般按额定风量的70%~80%选用。
1.2.3 本条规定了医药洁净室在划分空气调节系统应遵照的各项要求。
1 净化空气调节系统不能与一般空气调节系统合并,因为净化空气调节系统末端风口上装有空气过滤器,而一般空气调节系统风口上无过滤器,空气过滤器风口在运行过程中阻力会增加,而一般空气调节系统的风口运行中的阻力不变,所以随着运行时间的增加,可能出现医药洁净室风量越来越小,并使医药洁净室的房间或区域的空气压力发生变化。同时还考虑到医药洁净室需要良好的密闭性,也不允许通过风道使医药洁净室与一般空调房间连通。
2 由于无菌生产区的洁净度级别,微生物控制,温度、湿度要求,消毒方式与消毒频率等方面较非无菌生产区均有较大差别,所以从工艺操作要求、空调系统的运行管理、维护与节能方面而言,服务于两个不同区域的净化空气调节系统应分开设置。
3 含有可燃、易爆或有害物质的生产区(如原料药生产中的提取、结晶等工序)所占面积较大时,从安全角度考虑,其空气调节系统应与其他空气调节系统分开。但在制剂生产中,遇有布置分散的小面积该类医药洁净室,当系统上采用足够的安全措施后,可合用一个空调送风系统。
5 由于一个净化空气调节系统只有一个送风参数,对于温度、湿度控制要求差别大的医药洁净室,若合并使用同一个空气调节系统,送风参数需要按照温、湿度要求高的确定,才能同时满足参数要求低的区域(除非在送风支管上另设二次空气处理设备),这样会造成不必要的能量耗费,所以对温度、湿度要求差别大的区域,宜设置不同的净化空气调节系统,以提供不同要求的送风参数。而有时系统区域较小,分开设置可能因空气调节系统过多而增加造价,在经过技术经济比较后也可合并设置。
另外,别与低级别的医药洁净室(如A/B级与C/D级)除了在洁净级别,温度、湿度要求不同外,分开设置将有利于医药洁净室净化空气调节系统的运行管理。再者,系统风量大时,由于总送风回风管、机组体积均占用空间较大,且对机组强度性能、安装及维护运行带来不利因素,建议宜分开设置。
其他因产品类别不同而需独立设置的净化空气调节系统,见本标准*9.6.1条。
1.2.4 本条为强制性条文。本条*2款关于病原体操作区的回风利用问题,我国药品GMP(2010年修订)附录3“生物制品”*二十二条规定:“……来自病原体操作区的空气不得循环使用”。按照此条款的要求,凡是涉及病原体操作的生产区域,无论其危害程度属于哪一类,均不能利用回风,由此造成净化空气调节系统能耗的增加,不利节能降耗的原则。
根据《*共和国药典》(2015版Ⅲ部)“生物制品生产检定用菌毒种管理规程”,生物制品生产检定用菌毒种的危害程度,按照《人间的病原微生物名录》为基础,根据病原微生物的性、感染后对个体或者群体的危害程度,分为四类:
类病原微生物:指能够引起人类或动物非常严病的微生物,以及我国尚未发现或已经宣布消灭的微生物。
第二类病原微生物:指能够引起人类或动物严病,比较*直接或间接在人与人、人与动物、动物与动物间传播的微生物。
第三类病原微生物:指能够引起人类或动物疾病,但一般情况下对人、动物或环境不构成严重危害,传播高风险有限,实验室感染后很少引起严病,并且具备有效的和预防措施的微生物。
第四类病原微生物:指在通常情况下不会引起人类或动物疾病的微生物。
根据现行国家标准《实验室生物安全通用要求》GB 19489和《生物安全实验室建筑技术规范》GB 50346的有关规定,实验室生物安全防护等级(BSL,biosafety level)按所操作的生物因子的危害程度分为,其中一级防护程度,防护程度。以此类推,一类病原体操作的生物安全防护等级为BSL-4,二类病原体操作的生物安全防护等级为BSL-3,三类病原体操作的生物安全防护等级为BSL-2,四类病原体操作的生物安全防护的等级为BSL-1。
根据“生物制品生产检定用菌毒种管理规程”及其附录可知,生物制品生产检定用的菌毒种,均属于第二类、第三类、第四类病原体,其相对应的生物安全防护等级分别为BSL-3、BSL-2、BSL-1。
根据现行国家标准《实验室 生物安全通用要求》GB 19489-2008*6.3.3.3条的要求:“(BSL-3实验室)不得使用实验室防护区排出的空气”(BSL-4实验室按照BSL-3执行)。而对于BSL-1、BSL-2实验室,则无此要求。
根据世界卫生组织(WHO)2004年颁布的实验室生物安全手册(Laboratory Biosafety Manual,Third Edition,2004),关于生物安全等级的要求见表7。
做净化工程之医药车间无尘室装修
大部分医药生产车间无尘室都有严格的无尘无菌要求,及恒温、恒湿的要求,不仅对内的温、湿度有严格的要求,而且对温度和相对湿度的波动范围也有严格的要求。
医药车间无尘室,医药无尘室装修,净化工程,无尘室的原则:禁尘、带尘、产尘。风淋室作为进入洁净室的缓冲通道之一,是控制带尘的净化设备之一,它可以限度地减少员工进出无尘洁净室所带来的污染问题。风淋室的两道门电子互锁,可以兼起气闸室的作用,阻止外界污染和未被净化的空气进入无尘洁净区域,达到生产车间所要求的生产洁净环境。
做净化工程之医药车间无尘室装修,医药车间无尘室的室内空气参数要求 :
(1)温湿度要求:温度一般为24+2℃,相对湿度为55+5%。
(2)新风量大。由于这类车间内,人员比较多,可以根据以下数值应取下列的值:非单向流洁净室总送风量的10-30%;补偿室内排风和保持室内正压值所需的新鲜空气量;保证室内每人每小时的新鲜空气量≥40m3/h。
(3)送风量大。为了满足洁净室内的洁净度及热湿平衡,需要较大的送风量,就300平方米的车间,吊顶高度为2.5米的,如果是万级,送风量就需要300×2.5×30=22500m3/h的送风量(换气次数,是≥25次/h);如果是十万级,送风量就需要300×2.5×20=15000m3/h的送风量(换气次数,是≥15次/h)
以上就是无尘室装修、无尘车间工程建造施工的一些基本标准,希望对大家有帮助,青岛洁净净化技术有限公司,从事净化工程行业多年,有着丰富的行业经验,电子厂、食品厂、制药厂、化妆品厂等行业的百级至三十万级无尘室设计施工,实验室、无菌室的净化,企业厂房通风、换气、除尘、地面(环氧、自流平、抗静电、PVC等)工程。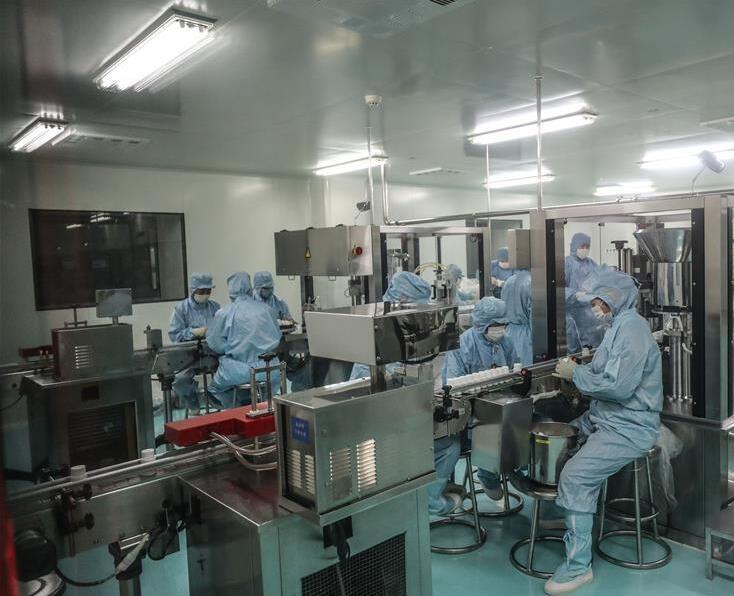
一个制药工厂的建设,整个建设过程中涉及很多的技术、工程规范、组织管理、过程控制、项目管理、政企关系……等方方面面的问题。总之,把一个制药工程项目做好,真的很难!
针对上述问题,国际制药项目管理协会(IPPM)和PharmLink倾情设计了“从一块土地到一个现代化药厂”的系列课程,广州、南京、济南、西安班,以一个个成功/失败的实例讲解了制药工厂/提取/口服药品项目建造的关键流程,并解答了大量实际项目中的各种疑难问题,数十家药企、高校、设计院的中高层工程、技术、管理人员参加了培训。
11月18-19日,IPPM和PharmLink拟在长春举办,并对课程进行了微调“从一块土地到一个现代化药厂”系列之二-提取车间及非无菌药品设计与建设流程实例详解。
结合实际案例及大量图纸详解、长时间互动答疑讨论,将是本次课程的特色。欢迎带上您的图纸、工艺流程,现场点评。
课题1 提取车间建造实例详解
1、案例分析:提取车间设计规划
2、提取车间项目设计思考
3、工艺难题与提取车间设计瓶颈
4、图纸案例分析:
1)某四层提取车间平面布局图
2)某二层前处理车间平面布局图
5、构建GEP与PPM体系,提高项目管理水平
6、提取车间设备选型与常见问题
7、提取/浓缩/醇沉/干燥模块设计关键
8、提取车间节能设计思考
9、提取自动化设计路径与方法要点
10、提取施工过程典型问题与注意事项
11、提取设备验证与工艺验证
12、典型GMP缺陷项分析
11月19日 09:00-15:30 (周二)
课题2 非无菌药品设备工艺/设计与建设流程实例详解
1、生产设备与工艺中的关键控制点
2、研发向生产转移要点及项目URS
3、制药工程概念设计要点
4、制药工程厂区布局要点
5、制药工程车间布局要点
6、非无菌药品工艺设计要点
7、人物流及洗衣中心设计图纸解析
8、备料及取样单元设计图纸解析
9、综合固体制剂车间设计案例解析
10、制药工程项目新改扩建工作流程及关键注意点
11、答疑
04
讲师介绍
张金巍
蒲公英创始人,硕士,,人力资源管理师,PMP,PPMP,天津市“131”创新人才,加拿大制药工程学院客座教授、PPM讲师,大型医药上市集团项目顾问,受邀国内外多家协会、高校、企业、GMP检查员等培训授课,专注提取、制药工程和项目管理18年。
焦红江
20多年制药行业经验,先后从事制药企业设备管理、生产管理、制药工程前期设计、制药工程项目管理等工作,具有丰富的GMP实施、GEP管理、制药工程设计、硬件疑难问题解决、厂房设施设备系统的确认验证、预防性维护、计量校准、计算机化系统验证……等经验,熟悉各种制药装备、生产工艺与自动化控制。先后参与或负责过10多个车间的GMP改造、多个FDA、欧盟cGMP认证项目,做过上百个车间的平面图纸审核、工艺概念设计、多家企业内训、现场模拟审计,现从事制药项目设计咨询、GMP咨询、工程项目管理、第三方验证外包服务。
医药无菌车间——洁净板项目工程案例
项目名称:济南瑞康医药无菌车间
应用板材:洁净板
应用系统:直接粘贴
施工时间:2017年6月
简 介:济南瑞康医药有限公司位于 临港经济开发区机场路东侧,是瑞康医药股份全资子公司。无菌车间装修项目使用墙冠UV氟碳洁净板共计2000㎡。
洁净板特性
1.防火
洁净板用特种硅酸钙板作为基板,燃烧性能达到GB8624A1级标准要求。当室内发生火灾时,能有效阻止火势的蔓延,不会产生有毒烟雾,无火焰传递;
2.环保
产品释放量符合GB18580-2001E1级,生产过程不使用任何溶剂,可挥发性**物(氡)<200Bq/m3,无氨,无笨,放射性达到A类装修材料标准。不含石棉;
3.
洁净板具有良好的性,抵抗多种病菌(大肠、金葡萄球菌、白色)在板材表面的存活;
4.耐腐蚀
洁净板具有相当的抵抗和二等各类腐蚀性物质的耐腐蚀性能,具有较强的耐酸、耐碱、的特性,包括各类清洁剂、消毒液及其它等;
5.耐候
基板品越,涂层经过十一次紫外光固化工艺,板材耐候性能强,使用寿命长达25年以上。具有防辐射、抗静电性能。
http://jamry.cn.b2b168.com
欢迎来到深圳市鑫诚丰净化装饰工程有限公司网站, 具体地址是广东省深圳市宝安区深圳市宝安区西乡大道256号乐群综合楼鹏宇达航空大厦5楼整层,联系人是吕经理。
主要经营深圳市鑫诚丰净化装饰工程有限公司主营: GMP洁净室净化装修、无菌室实验室装修、口罩无尘车间装修。价格优惠。欢迎广大用户前来选购。
。
单位注册资金单位注册资金人民币 250 - 500 万元。
这里价格实惠,这里生活服务齐全,我们的服务有:GMP洁净室净化装修,口罩无尘车间装修价格,无菌室实验室装修价格!欢迎前来合作!